Современные способы хирургического лечения заболеваний сердца
Современные способы хирургического лечения заболеваний сердца
Хирургические методы лечение ишемической болезни сердца (ИБС) — реваскуляризация миокарда
Медикаментозные (лекарственные) методы лечения ИБС направлены, главным образом, на снижение потребления миокардом кислорода и, следовательно, на выравнивание дисбаланса между его доставкой и потреблением. В отличие от этого, хирургические методы лечения ИБС имеют своей целью прямое увеличение коронарного кровотока – реваскуляризация миокарда. Эта цель может быть достигнута двумя путями:
– обходным шунтированием коронарных артерий — операция аортокоронарного шунтирования (АКШ),
– чрескожные коронарные вмешательства (ЧКВ) или ангиопластика и стентирование коронарных артерий, направленной непосредственно на область сужения коронарного сосуда.
Аортокоронарное шунтирование (АКШ) или коронарное шунтирование (КШ) – операция, позволяющая восстановить кровоток в артериях сердца (коронарных артериях) путём обхода места сужения коронарного сосуда с помощью шунтов.
Современная хирургия ишемической болезни сердца возникла сравнительно недавно. Первые операции прямой реваскуляризации миокарда были выполнены в 60-е годы ХХ века. Многочисленные сравнительные исследования убедительно доказали, что операции прямой реваскуляризации миокарда (КШ) увеличивают продолжительность жизни, снижают риск развития инфаркта миокарда и улучшают качество жизни по сравнению с медикаментозной терапией, особенно в группах больных с прогностически неблагоприятным поражением коронарного русла.
Внедрение в практику чрескожных методов реваскуляризации – коронарной ангиопластики – начато с 1977 года, когда А. Грюнтциг впервые выполнил транслюминальную баллонную ангиопластику критического сужения нативной коронарной артерии.
Транслюминальная баллонная ангиопластика (ТЛБАП) – операция, позволяющая восстановить кровоток в артериях сердца (коронарных артериях) путём проведения катетера с баллоном и последующем его раздуванием. Операция ТЛБАП сопровождалась высоким риском осложнений в виде повторного сужения сосуда – рестеноза, острых окклюзий.
В 1986 году У. Сигварт и Ж. Пуэл открыли эру эндопротезирования венечных артерий, имплантировав первые стенты в коронарное русло. Стент – внутрисосудистый протез для поддержания стенки пораженного сосуда и сохранения диаметра его просвета. Конструкция стента представляет собой тонкий сетчатый каркас из инертного металлического сплава высочайшего качества, раскрываемый баллоном внутри сосуда до нужного диаметра.
Положительные результаты рандомизированных исследований сделало стентирования коронарных артерий ведущим стандартом в лечении больных ИБС. С 1999 году под термином чрескожное коронарное вмешательство «по умолчанию» подразумевать именно стентирование коронарных артерий.
Стентирование коронарных артерий или чрескожное коронарное вмешательство – операция, позволяющая восстановить кровоток в артериях сердца (коронарных артериях) путём имплантации стентов в месте сужения коронарной артерии.
Проблема хирургического лечения больных ишемической болезни сердца остается одной из наиболее актуальных и приоритетных задач мирового и отечественного здравоохранения.
Интервенционные методы в лечении сердечно-сосудистых заболеваний
Стельмашок Виталий Иванович, заведующий лабораторией неотложной и интервенционной кардиологии РНПЦ «Кардиология», кандидат медицинских наук
В настоящее время сердечно-сосудистые заболевания являются основными причинами смертности населения в развитых странах мира. К сожалению, Республика Беларусь здесь не является исключением: так, согласно данным статистической отчетности, в нашей стране сердечно-сосудистая патология является абсолютным лидером по вкладу в показатель общей смертности — более половины от общего числа летальных исходов случаются по причине болезней системы кровообращения.
Ишемическая болезнь сердца относится к числу наиболее значимых сердечно-сосудистых заболеваний — на долю ее различных форм приходится приблизительно 2/3 смертей от общего числа летальных исходов по причине сердечно-сосудистых заболеваний. Суть ишемической болезни сердца состоит в том, что в коронарных артериях, кровоснабжающих сердечную мышцу, вследствие прогрессирования атеросклероза происходит рост и развитие атеросклеротических бляшек. При наличии стабильных бляшек происходит постепенный их рост, приводящий к сужению просвета артерии (см. рис. 1), к нарушению кровотока по данной артерии и к кислородному голоданию (ишемии) находящихся в зоне кровоснабжения данной артерии органов и тканей. Клинически это проявляется наличием стабильной стенокардии различной степени тяжести.
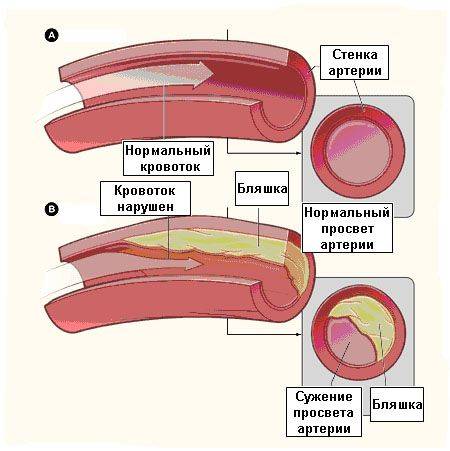 |
Рис. 1. Непораженная коронарная артерия (а), стабильная атеросклеротическая бляшка (б), вызывающая сужение просвета сосуда
В свою очередь, нестабильные атеросклеротические бляшки являются «ранимыми», склонными к разрыву, что ведет к появлению тромба на поверхности разорвавшейся атеросклеротической бляшки (см. рис. 2), к острому нарушению кровотока по данной артерии, что клинически проявляется развитием нестабильной стенокардии или же инфаркта миокарда.
Несмотря на значительные успехи медикаментозной терапии, применяемой для лечения пациентов, страдающих ишемической болезнью сердца, данный вид лечения не всегда способен в полной мере решить поставленные задачи, которые заключаются в улучшении качества (то есть уменьшение тяжести и числа эпизодов стенокардии) и в увеличении продолжительности жизни пациентов. В данных случаях на помощь медикаментозной терапии приходят интервенционные и хирургические методы лечения данного заболевания.
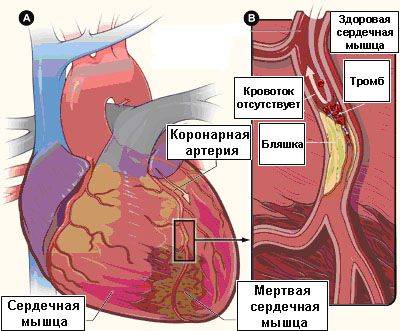 |
Рис. 2. Сердце (а), разорвавшаяся нестабильная атеросклеротическая бляшка с тромбом на ее поверхности (б),
приводящие к прекращение кровотока за зоной бляшки и к развитию омертвения части сердечной мышцы
В том случае, когда планируется хирургическое или интервенционное вмешательство у больного, страдающего ишемической болезнью сердца, необходимо проведение специального инвазивного исследования, называемого коронарографией. Данная процедура нужна для того, чтобы точно оценить характер поражения коронарных артерий, что позволит выбрать наиболее оптимальную тактику дальнейшего лечения — выполнение малоинвазивных вмешательств, таких как чрескожная баллонная ангиопластика/стентирование коронарных артерий или же «большой» операции — аортокоронарного шунтирования. Следует отметить, что проведение коронарографии особенно необходимо пациентам с ишемической болезнью сердца, у которых имел место перенесенный инфаркт, или же стенокардия плохо поддается медикаментозному лечению.
Процедура коронарографии выполняется под местной анестезией, после которой проводится пункция крупной магистральной артерии на ноге или же на руке. Затем в пунктированную артерию устанавливается специальная трубка — интрадьюсер, через которую в аорту, а затем в устье коронарных артерий проводятся специальные катетеры. Через данные катетеры в артерии сердца вводят специальное рентгеноконтрастное вещество, которое током крови разносится по коронарным сосудам, и делает их видимыми для специальной установки — ангиографа, который показывает весь результат на экране монитора. Поэтому, где, как и насколько поражены сосуды сердца, видно очень хорошо. Особо следует отметить, что во время процедуры пациент не чувствует никаких болевых ощущений (в сосудах нет болевых рецепторов), находится в сознании и может наблюдать за картиной его собственных коронарных артерий, выводимых на монитор ангиографического аппарата. Процедуры коронарографии, а также других диагностических и лечебных миниинвазивных вмешательств на сосудах выполняются специальными врачами — рентгенэндоваскулярными хирургами.
Бояться коронарографии не стоит — это важная диагностическая процедура. В некоторых случаях, крайне редко, возможны осложнения (нарушение ритма сердца, аллергия на контрастное вещество, тромбоз артерии и т.д.), но они всегда поддаются экстренной помощи.
Ангиопластика и стентирование коронарных артерий — самые щадящие методы хирургического лечения суженных сосудов. Данная процедура, как и коронарография, является безболезненной и проводится под местной анестезией (пациент находится в сознании). В настоящее время ежегодно во всем мире выполняется более 2 млн. подобных процедур.
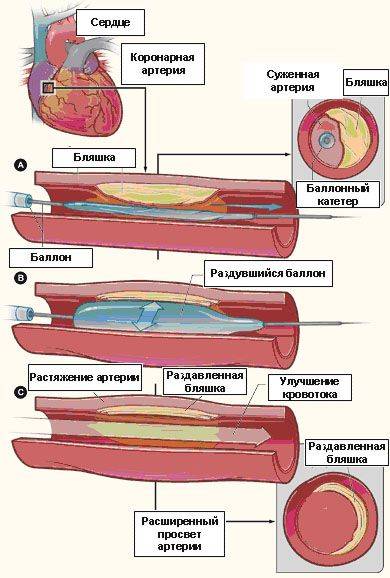 |
Рис. 3. Нерасправленный баллонные катетер позиционирован в зоне сужения коронарной артерии (а), раздутие баллона,
приводящее к фрагментации бляшки (б), полное восстановление проходимости коронарной артерии (с)
Начинается процедура ангиопластики/стентирования коронарных артерий с проведения под рентгеновским контролем и установке в устье коронарной артерии особого инструмента — направляющего катетера. После того, как направляющий катетер установлен в устье коронарной артерии, по нему в сосуд проводится тонкий проводник диаметром около 0,35 мм, таким образом, что его кончик находится за зоной сужения. Затем в сосуд по проводнику вводится специальный баллонный катетер, который позиционируется в зоне сужения сосуда. После этого врач раздувает баллон (обычно до 10-14 атмосфер) в течение 20-30 сек, и просвет сосуда расширяется, после чего баллонный катетер сдувается и извлекается из просвета сосуда (см. рис. 3).
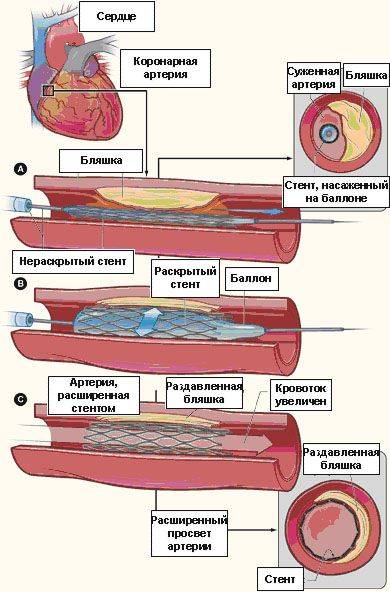 |
Рис. 4. Насаженный на баллоне стент позиционирован в зоне сужения коронарной артерии (а),
раздутие баллона с имплантацией стента (б), полное восстановление проходимости коронарной артерии (с)
С целью предупреждения развития повторного сужения леченного сосуда (рестеноза) рентгенэндоваскулярный хирург практически всегда после удаления баллонного катетера устанавливает в расширенное место сосуда стент — проволочную конструкцию цилиндрической формы, служащую каркасом для данного участка артерии. Коронарный стент насажен на баллон, который находится в нераскрытом состоянии, и в таком виде по проводнику проводится к пораженному месту артерии. После того, как врач четко выполнит позиционирование стента в нужном участке сосуда, производится раздутие баллона, на котором насажен стент (обычно до 12-20 атмосфер), в процессе которого стент расширяется и плотно прижимается к сосудистой стенке (см. рис. 4). Затем врач сдувает баллон и удаляет его из сосуда, а раскрывшийся стент остается в просвете сосуда пожизненно. Заканчивается процедура ангиопластики/стентирования коронарных артерий удалением проводника, катетера и интрадьюсера из сосудистого русла. Место прокола сосуда прижимается для остановки кровотечения либо закрывается при помощи специальных устройств. В среднем длительность процедуры ангиопластики/стентирования коронарных артерий занимает от 45 минут до 3 часов.
Однако даже стентирование не дает стопроцентной гарантии исключения рестеноза. Дело в том, что со временем стент обрастает соединительной тканью и вновь происходить сужение просвета артерии. Поэтому в тех случаях, когда у пациента ожидаемо высокий риск развития рестеноза, имплантируются специальные стенты с лекарственным покрытием, выделяющие антипролиферативные препараты, которые подавляют рост соединительнотканных компонентов.
Следует также помнить о том, что после процедуры ангиопластики/стентирования коронарных артерий пациент должен постоянно принимать специальную терапию. Во-первых, это касается антитромбоцитарных препаратов, способствующих разжижению крови: аспирин — постоянно и клопидогрель в течение 1-12 месяцев. В случае имплантации стентов с покрытием, выделяющими антипролиферативные препараты, длительность приема клопидогреля увеличивается до 12-24 месяцев. Помимо вышеуказанного, необходимо пожизненно принимать статины (препараты, снижающие уровень холестерина) — это является надежным методом профилактики роста атеросклеротических бляшек в других участках коронарных артерий. Также необходимо принимать медикаментозную терапию, предназначенную для лечения ишемической болезни сердца и, при необходимости, лекарства, снижающие артериальное давление. Регулярный и правильный прием медикаментозной терапии под контролем врача-кардиолога — залог успеха на будущее.
Однако не следует полагать, что проведение процедуры ангиопластики/стентирования возможно только в пораженных атеросклерозом артериях сердца. В настоящее время разработаны и успешно применяются специальные баллонные катетеры и стенты для лечения пораженных атеросклерозом сонных артерий, почечных артерий, висцеральных артерий и артерий нижних конечностей; специальные протезы (стент-графты) используются для лечения аневризм аорты. Широко в клинической практике применяются различного типа окклюдеры, которые нужны для устранения врожденных дефектов межпредсердной и межжелудочковой перегородок сердца; разрабатываются специальные клапаны, которые в будущем можно будет имплантировать миниинвазивно, без остановки сердца, что позволит избежать выполнения «большой» операции у некоторых пациентов, страдающих пороками сердца. Уже сейчас с большой долей вероятности можно утверждать, что в последующие годы показания к применению интервенционных методов для лечения сердечно-сосудистых заболеваний будут только расширяться, а данные процедуры проводиться все чаще и чаще.
На сегодняшний день в Республике Беларусь головным учреждением, где происходит разработка и внедрение новых интервенционных методов в клиническую практику для лечения больных с сердечно-сосудистой патологией, является Республиканский научно-практический центр «Кардиология». Высококвалифицированный персонал работающих в центре врачей рентгенэндоваскулярных хирургов выполняет сложные и высокотехнологичные миниинвазивные диагностические и лечебные процедуры на сердце и сосудах на высоком профессиональном уровне с хорошими ближайшими и отдаленными результатами.
220036, Республика Беларусь, г. Минск, ул. Р. Люксембург, 110Б
СОВРЕМЕННЫЕ ПОДХОДЫ
К ЛЕЧЕНИЮ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА
Ю. И. Бузиашвили, доктор медицинских наук, профессор,
научный центр сердечно-сосудистой хирургии им. А.Н. Бакулева РАМН
Последние данные медицинской статистики неутешительны: они свидетельствуют о росте сердечно-сосудистых заболеваний у населения России. Ишемическая болезнь сердца занимает сегодня 30% в структуре заболеваемости россиян и около 36% – среди причин общей смертности. Распространение этого грозного заболевания приобрело уже характер эпидемии.
Боль в груди – весьма частая жалоба, и во многих случаях она не связана с заболеванием сердца. Однако для значительного числа пациентов появление такой боли означает поражение коронарных артерий. Изменения в артериях являются основной причиной ишемической болезни сердца (ИБС).
А начинается этот процесс с патологических изменений во внутренней стенке артерии, кровоснабжающей сердечную мышцу, что приводит к формированию атеросклеротических бляшек. Со временем размеры бляшек увеличиваются, и происходит сужение просвета коронарной артерии. В результате затрудняется кровоток по пораженному сосуду, и определенный участок сердечной мышцы перестает получать достаточное количество кислорода для нормальной работы. На этом этапе и появляются симптомы заболевания, которое в народе окрестили «грудной жабой», а в медицинской литературе назвали «стенокардией». Стенокардия является не самостоятельным заболеванием, а проявлением или симптомом ишемической болезни сердца.
Сердце перекачивает кровь, необходимую для жизнедеятельности всего организма. Ежедневно сердце сокращается до 100 тысяч раз и более 2 биллионов раз в течение жизни! Так же, как и другие ткани организма, сердце нуждается в кислороде для обеспечения своей активности. Любая нагрузка, физическая или эмоциональная, может вызвать резкое повышение активности сердца, что увеличивает потребность миокарда (сердечной мышцы) в кислороде. Когда коронарная артерия сужена на 50 и более процентов, это может привести к стенокардии.
Как правило, на начальных стадиях болезни признаки стенокардии дают о себе знать при высоких физических нагрузках и сильных эмоциональных переживаниях. При этом за грудиной или в левой половине грудной клетки появляются боли давящего, сжимающего характера, которые могут отдавать в левую руку, лопатку, левое плечо, нижнюю челюсть и т.д. В покое боли постепенно проходят. Также заболевание может сопровождаться неприятными ощущениями в грудной клетке, чувством дискомфорта или нехватки воздуха (что иногда трактуется как одышка), ощущением «кома в горле».
Постепенно болезнь прогрессирует. Человек все хуже переносит физические нагрузки и вынужден обратиться к врачу. С этого момента считавший себя здоровым человек будет постоянно посещать кардиолога и принимать различные препараты. Несмотря на проводимое годами и подчас дорогостоящее лечение, те же жалобы начинают беспокоить пациента и в состоянии покоя – при чтении, просмотре телевизора, после еды, по ночам. Большинство пациентов полностью теряют свою трудоспособность. Кроме того, за время болезни очень многие переносят инфаркты миокарда (смерть части сердечной мышцы) различной степени тяжести.
К большому сожалению, кардиологи рассматривают возможность хирургического лечения, когда консервативная терапия уже не помогает. Однако давность заболевания и имеющиеся осложнения значительно ухудшают прогноз, а зачастую делают хирургическое лечение невозможным. Поэтому чем раньше поставлен диагноз и предприняты рациональные методы лечения, тем больше вероятность вернуть пациенту трудоспособность, значительно улучшить «качество» его жизни и предотвратить развитие такого грозного заболевания, как инфаркт миокарда, и сопутствующих ему осложнений.
У людей часто возникают вопросы: какие существуют современные методы хирургического лечения ишемической болезни сердца, как и зачем выполняется та или иная операция, каков риск ее выполнения? Постараюсь ответить на эти вопросы подробнее.
Наиболее часто сегодня выполняется операция аортокоронарного шунтирования (AKШ). Благодаря технологическим разработкам последних лет она считается высокоэффективной процедурой, проверенной временем. Существуют много причин, по которым может быть рекомендовано АКШ: если на фоне медикаментозной терапии уже не удается уменьшить симптомы стенокардии, если имеется опасное для жизни поражение коронарных артерий, если у пациента есть осложнения, связанные с перенесенным инфарктом миокарда. Целью оперативного вмешательства является шунтирование (обход) пораженной артерии здоровым сосудом, взятым с ноги пациента или с грудной стенки. Каждый шунт увеличивает поступление крови к сердечной мышце и способствует уменьшению боли в груди. Число таких шунтов зависит от количества пораженных у пациента коронарных артерий.
АКШ выполняется высококвалифицированной бригадой кардиохирургов. Во время операции аппарат искусственного кровообращения берет на себя функции сердца и легких, позволяя хирургу пришить шунт к пораженной артерии на остановленном сердце. Операция длится от 2 до 6 часов. Компьютеризированные мониторы, которые следят за работой сердца во время АКШ, и новейшие кардиологические препараты обеспечивают благоприятный исход операции. Однако врач предварительно обсуждает с пациентом и возможный риск: осложнения со стороны легких, послеоперационные кровотечения, инфаркт миокарда, осложнения со стороны головного мозга.
Во многих случаях проведение аортокоронарного шунтирования невозможно: когда у человека тонкие, не поддающиеся шунтированию артерии, множественные атеросклеротические бляшки, расположенные по ходу всей артерии, полностью закрытые артерии и т.д. Буквально несколько лет назад такие пациенты считались неоперабельными. В настоящее время им могут порекомендовать проведение трансмиокардиальной лазерной реваскуляризации (ТМЛР). Это новый вид хирургического лечения ишемической болезни сердца, при котором используется лазерная энергия высокой мощности.
Основой данной операции является создание лазером специальных каналов, по которым кровь поступает непосредственно из полости левого желудочка в миокард, тем самым осуществляя кровоснабжение (доставку кислорода) в пораженные участки сердца. Кроме того, операция стимулирует рост новых мелких кровеносных сосудов (коллатеральной сети) в сердечной мышце, что уменьшает проявления стенокардии и улучшает работу сердца.
В каждом отдельном случае хирург решает, какое количество каналов (перфораций) надо сделать. Обычно делают 20–30 перфораций. Но если операция выполняется совместно с аортокоронарным шунтированием (когда хотя бы одну артерию можно шунтировать), каналов может быть меньше. Они, как правило, не превышают в диаметре 1 мм: это чуть больше диаметра стандартных игл для шитья.
Пациенту необходимо знать, что, в отличие от АКШ, эта операция не рассчитана на непосредственный эффект. Типичные боли могут исчезнуть буквально на 2–3 день после хирургического вмешательства, могут уменьшиться, но могут и остаться прежними. Даже к концу первого месяца пациент может не ощутить значительных изменений. Однако к третьему месяцу после операции ситуация начинает меняться: количество приступов стенокардии уменьшается, их интенсивность снижается. К шестому месяцу физическая активность пациента заметно возрастает. Если он будет четко следовать плану реабилитации, то добьется оптимальных результатов.
Наиболее точную информацию о локализации и протяженности атеросклеротических бляшек в сосудах сердца дает коронарная ангиография.
Процедура выполняется в специальной рентгеноперационной под местной анестезией и длится не более 20–25 минут. Через артерию на ноге или руке пациента проводится тонкий пластиковый катетер к сосудам сердца. По катетеру поступает контрастное вещество. В момент его введения делается рентгеновская съемка, при которой хорошо видны сосуды сердца. В некоторых операционных у пациента есть возможность наблюдать весь ход исследования на мониторе.
В настоящее время применение новейшей аппаратуры и современных контрастных веществ (большинство из которых не вызывают аллергических реакций и быстро выводятся из организм) делают коронографию базопасной и надежной.
Многие пациенты с ишемической болезнью сердца могут лечиться при помощи ангиопластики – щадящей техники, также улучшающей приток крови к сердцу. Транслюминалыная баллонная ангиопластика (ТЛБАП) длится около двух часов, выполняется под местной анестезией, позволяет «встать на ноги» в течение нескольких дней и вести активный образ жизни. При проведении ангиопластики в бедренную артерию проколом через кожу вводят специальное устройство, через которое продвигают к сердцу узкую трубку – проводниковый катетер. По нему подается контрастное вещество, позволяющее врачу видеть сосуды сердца на экране монитора. Следя за изображением на экране, доктор вводит баллонный катетер и помещает баллон в месте стеноза (сужения артерии).  Баллон раздувается и, расширяясь, вдавливает атеросклеротическую бляшку в стенки артерии. Затем баллон сдувают и удаляют. Кровь по сосуду вновь поступает к сердцу. Пациент, находясь в полном сознании, может наблюдать за всем ходом операции.
Баллон раздувается и, расширяясь, вдавливает атеросклеротическую бляшку в стенки артерии. Затем баллон сдувают и удаляют. Кровь по сосуду вновь поступает к сердцу. Пациент, находясь в полном сознании, может наблюдать за всем ходом операции.
Примерно в 25–30% случаев после успешно проведенной ангиопластики стеноз может возникнуть снова. Это называется рестеноз. В этом случае пациенту может быть рекомендована еще одна процедура – имплантация коронарного стента.
Стент – это каркасная трубка сетчатой структуры из нержавеющих металлов. Размеры стента подбираются индивидуально в зависимости от размера артерии. На специальном баллоне стент проводится в нужный сегмент пораженного сосуда. Баллон раздувается, и стент, расправляясь, плотно прилегает к стенкам коронарной артерии, механически препятствуя ее сужению и сохраняя восстановленный кровоток к сердцу.  Стент остается в месте стеноза постоянно, удерживая артерию открытой. Стентировать можно одну и более артерий. Также в одном сосуде может быть установлено несколько стентов.
Стент остается в месте стеноза постоянно, удерживая артерию открытой. Стентировать можно одну и более артерий. Также в одном сосуде может быть установлено несколько стентов.
В большинстве случаев ангиопластика и стентирование проводятся достаточно быстро, легко и без неприятных ощущений. Однако, как любая операция на сердце, они могут иметь осложнения (примерно 5%). Поэтому во время проведения этих процедур наготове должна находиться хирургическая бригада для выполнения экстренной операции аорто-коронарного шунтирования. У одного и того же пациента ангиопластика или стентирование могут выполняться неоднократно. Только в случае частых рестенозов или прогрессирования заболевания и вовлечения в процесс других коронарных артерий может встать вопрос об открытой операции на сердце.
Поликлиника № 4 2004 год (стр. 36)
Современные немедикаментозные методы лечения стабильной ИБС — наружная контрпульсация

Современные немедикаментозные методы лечения стабильной ИБС

Современные аппаратные комплексы для проведения НКП включают в себя: управляемую компьютером пневматическую систему, три пары пневматических манжет, монитор ЭКГ, АД, а также пальцевой плетизмограф. Во время сеанса контрпульсации на икры, нижнюю и верхнюю часть бедер пациента накладываются 3 пары пневматических манжет, последовательно надуваемых сжатым воздухом от периферии к центру. Триггером для надувания и сдувания манжет является зубец R на ЭКГ, который анализируется микропроцессором. Результатом этого является повышение диастолического давления в аорте и увеличение коронарного перфузионного давления, а также разгрузка левого желудочка во время систолы.

Комбинация этих процессов может привести к снижению потребности миокарда в кислороде, увеличению коронарного кровотока и сердечного выброса, что положительно влияет на пациентов с клиническими проявлениями стенокардии.
Проспективные клинические исследования и регистры с участием большого количества пациентов свидетельствуют о значительном снижении симптомов стенокардии и улучшении объективных показателей функции миокарда у больных, прошедших курс НКП. Это послужило основанием для включения наружной контрпульсации, в качестве альтернативного метода лечения рефрактерной стенокардии, в руководство ACC/AHA по лечению пациентов с хронической стабильной стенокардией.
Как проводится наружная контрпульсация?
Во время сеанса наружной контрпульсации Вы ложитесь на кушетку; на бедра и голени, в некоторых моделях и на руки, накладываются пневматические манжетки. На грудь накладываются электроды для постоянной записи электрокардиограммы (ЭКГ), которая выводится на экран монитора. На палец надевается датчик для записи кривой пульса, отображающей кровоток в артериях; кроме того, с помощью датчика измеряется насыщение крови кислородом. Во время процедуры манжетки на ногах и руках последовательно надуваются и сдуваются синхронизировано с сердечным ритмом. Во время диастолы, когда сердечная мышца расслаблена и наполняется кровью, а также происходит наполнение коронарных артерий, манжетки последовательно (снизу-вверх) надуваются.

Это приводит к формированию волны крови, направленной к сердцу, что улучшает кровоток в коронарных сосудах. Затем в систолу, когда сердечная мышца сокращается и выбрасывает кровь в аорту, манжетки резко сдуваются. Это облегчает работу сердца и ускоряет кровоток в остальных сосудах.
Курс лечения рассчитан на 35 ч в режиме 1-2 часа ежедневно в течение 4-7 недель.
Кто является кандидатом для наружной контрпульсации?
Возможно, Вам показана наружная контрпульсация, если:
• Вы страдаете хронической ишемической болезнью сердца;
• Вы не получаете облегчения от приема препаратов, в том числе нитратов;
• По каким-либо причинам Вам противопоказана ангиопластика и аортокоронарное шунтирование.
Противопоказания к наружной контрпульсации
• Острая сердечная недостаточность;
• Недостаточность аортального клапана;
• Некоторые нарушения ритма сердца;
• Повышенное артериальное давление, неконтролируемое лекарственными препаратами;
• Тромбоз (закупорка) глубоких вен ног;
• Повышенная кровоточивость;
• Беременность;
• Онкологические заболевания
Возможные осложнения наружной контрпульсации:
Усиленная наружная контрпульсация – процедура неинвазивная, поэтому риск развития каких-либо осложнений крайне невелик. Наиболее частыми проблемами после курса наружной контрпульсации являются повреждения кожи, гематомы на месте накладывания манжет. Некоторые пациенты отмечают боли в ногах после процедуры.
Каталог
Элемент не найден!
Электронная подписка
Для получения доступа к тексту статей журнала воспользуйтесь услугой «Электронная подписка»:
Главный редактор
Лео Антонович Бокерия, доктор медицинских наук, профессор, академик РАН и РАМН, директор ФГБУ «НМИЦССХ им. А.Н. Бакулева» МЗ РФ
Академик РАН и РАМН Лео Антонович БОКЕРИЯ,
директор «НМИЦССХ» им. А.Н. Бакулева,
главный редактор издательства Центра
Кардиохирург, ученый, педагог и организатор науки, доктор медицинских наук (1973 г.), профессор (1982 г.), академик РАМН (1994 г.), академик РАН (2011 г.), заслуженный деятель науки РФ (1994 г.), лауреат Ленинской премии (1976 г.), Государственной премии СССР (1986 г.), Государственной премии РФ (2002 г.), Премии Правительства РФ (2003 г.).
В 1994 г. Л.А. Бокерия избран по конкурсу на должность директора НМИЦССХ им. А.Н. Бакулева. В 1998 г. одновременно становится директором Центра хирургической и интервенционной аритмологии МЗ РФ.
С 1994 г. является заведующим кафедрой сердечно-сосудистой хирургии Российской медицинской академии последипломного образования (РМАПО) МЗ РФ. С 1995 г. заведует созданной им кафедрой сердечно-сосудистой хирургии № 2 Московской медицинской академии (ныне Первого МГМУ) им. И.М. Сеченова МЗ РФ.
С 2003 г. возглавляет кафедру сердечно-сосудистой хирургии и интервенционной кардиологии Московского государственного медико-стоматологического университета им. А.И. Евдокимова МЗ РФ.
По инициативе Л.А. Бокерия в НМИЦССХ успешно функционирует учебно-исследовательский центр «Современные медицинские технологии», который ежегодно проводит 4–6 курсов последипломного повышения квалификации специалистов высшего звена.
Л.А. Бокерия выполняет весь известный арсенал операций на сердце при самой разнообразной патологии: от 3 до 6 операций в день, то есть от 700 до 900 операций с использованием искусственного кровообращения в год.
С 1996 г. он является главным кардиохирургом МЗ РФ.
Л.А. Бокерия – автор и соавтор свыше 3700 научных публикаций, в том числе более 250 книг, более 100 изобретений и полезных моделей, более 300 программ и баз данных для ЭВМ, ряд которых зарегистрированы за рубежом, по различным проблемам сердечно-сосудистой хирургии, кардиологии, медицинского образования и организации медицинской науки.
Л.А. Бокерия принадлежат уникальные работы по теоретическому обоснованию и клиническому использованию метода гипербарической оксигенации в хирургии сердца и сосудов. Он крупнейший специалист в области диагностики и хирургического лечения нарушений ритма и проводимости сердца (особенно тахиаритмий), включая различные сочетания сердечных аритмий с врожденными и приобретенными пороками и аномалиями развития сердца, коронарной болезнью.
Л.А. Бокерия является инициатором развития и другого нового раздела кардиохирургии в нашей стране – минимально инвазивной хирургии сердца. Большой вклад внес Л.А. Бокерия в решение проблемы хирургического лечения ИБС.
Велика роль Л.А. Бокерия в разработке новых подходов к хирургическому лечению терминальной сердечной недостаточности. Его заслугой является разработка новых операций у тяжелой категории кардиохирургических больных с различными формами кардиомиопатий. Он первым развил концепцию динамической кардиомиопластики, в том числе и у детей. Л.А. Бокерия выполнил первую в нашей стране имплантацию искусственного желудочка сердца и после большого перерыва инициировал возобновление в Центре выполнения операций по трансплантации сердца.
По инициативе Л.А. Бокерия в клиническую практику внедрены передовые технологии диагностики и реконструктивной хирургии заболеваний восходящего отдела и дуги аорты.
Он генерировал развитие и другого направления современной медицинской науки – креативной кардиологии, которая определяет необходимость созидательного сотрудничества врачей разных специальностей: кардиологов, кардиохирургов, специалистов по функциональной диагностике, фундаментальным и прикладным дисциплинам.
Под руководством Л.А. Бокерия в Центре разрабатываются и внедряются в клиническую практику новые высокотехнологичные принципы профилактики и лечения больных с сердечно-сосудистой патологией – использование методов генной и клеточной терапии.
Академик Л.А. Бокерия проводит приоритетные исследования по созданию биопротезов клапанов сердца для коррекции клапанных пороков – низкопрофильного, изогнутого по плоскости биопротеза митрального и трикуспидального клапанов, воспроизводящего естественную форму фиброзного кольца, на упругоподатливом каркасе. Продолжено изучение эффективности защиты миокарда у детей первого года жизни при применении нового внутриклеточного кардиоплегического раствора «Бокерия – Болдырева», созданного в НМИЦССХ под руководством Л.А. Бокерия.
Л.А. Бокерия активно занимается методологией медицинской науки и педагогической деятельностью. Он является создателем крупнейшей в стране кардиохирургической школы, воспитавшим не одно поколение врачей – кардиохирургов, кардиологов, реаниматологов и специалистов других смежных специальностей.
Л.А. Бокерия – научный руководитель 350 кандидатских и консультант более 100 докторских диссертаций. Он создатель издательства НМИЦССХ им. А.Н. Бакулева с типографией, основатель и главный редактор журналов «Анналы хирургии», «Бюллетень НМИЦССХ им. А.Н. Бакулева «Сердечно-сосудистые заболевания», «Детские болезни сердца и сосудов», «Клиническая физиология кровообращения», «Анналы аритмологии», «Креативная кардиология», информационного сборника «Сердечно-сосудистая хирургия»; главный редактор журнала «Грудная и сердечно-сосудистая хирургия».
Активная деятельность Л.А. Бокерия и его вклад в отечественное здравоохранение отмечены званиями и премиями самого высокого достоинства. Он лауреат Ленинской премии (1976 г.), двух Государственных премий (1986 г. – СССР, 2002 г. – РФ), Премии Правительства Российской Федерации (2003 г.). За выдающиеся достижения Л.А. Бокерия награжден орденом «За заслуги перед Отечеством» III (1999 г.), II (2004 г.) и IV (2010 г.) степени, орденом Достоинства и Чести (Республика Грузия, 1999 г.), орденом Преподобного Сергия Радонежского II степени (2001 г.). Русский биографический институт неоднократно признавал Л.А. Бокерия «Человеком года», а в 2000 г. – «Человеком десятилетия» в номинации «Медицина». В 2002 г. он удостоен титула «Человек-легенда», общероссийской премии «Русский национальный Олимп», учрежденной Правительством, Союзом промышленников и фондом «Третье тысячелетие». Как одному из ведущих кардиохирургов мира в 2003 г. Л.А. Бокерия вручена международная премия «Золотой Гиппократ». В 2004 г. он удостоен премии РАН «Триумф» в номинации «Наука о жизни – медицина». В 2004 г. он отмечен наградным знаком – орденом «Меценат», который присуждается Благотворительным фондом «Меценаты столетия» за выдающийся вклад в дело возрождения и процветания мира, за величие души, за бескорыстную щедрость; в 2004 и 2005 г. – Золотым почетным знаком «Общественное признание», который присуждается Национальным фондом «Общественное признание», Национальным гражданским комитетом по взаимодействию с правоохранительными, законодательными и судебными органами и независимой организацией «Гражданское общество» за большой личный вклад в развитие отечественной медицины, проведение уникальных кардиохирургических операций с применением новейших медицинских технологий, спасших жизни сотен детей и новорожденных, многолетнюю и плодотворную научно-практическую, педагогическую и просветительскую деятельность, активную гражданскую позицию.
В 2006 г. Л.А. Бокерия награжден Почетным алмазным орденом «Общественное признание», удостоен диплома Президиума Парламента народов России «за спасение многочисленных жизней, выдающиеся знания, умение руководить, за уникальные личные качества – благородство, мужество, чувство долга, умение беречь честь и достоинство, держать слово и делать дело, в также за веру в великое будущее Отечества», Золотой медали – за выдающийся вклад в образование России и Золотой звезды «Честь, гордость и слава России».
В 2008 г. Л.А. Бокерия награжден медалью «За практический вклад в укрепление здоровья нации», Орденом Чести с присуждением звания «Опора честного бизнеса» и почетного титула «Выдающийся кардиохирург современности». В 2009 г. огромный вклад Л.А. Бокерия в науку и отечественное здравоохранение отмечен присуждением ему Премии имени А.Н. Косыгина «За большие достижения в решении проблем развития экономики России» и премии города Москвы в области медицины «за разработку и внедрение в клиническую практику нового биологического клапана «Биоглис».
Л.А. Бокерия – действительный член Американской ассоциации торакальных хирургов (1991 г.), член правления (1992 г.) и член Президиума (с 2003 г., консул) Европейского общества грудных и сердечно-сосудистых хирургов, член правления Европейского общества сердечно-сосудистых хирургов, член научного правления Международного кардиоторакального центра Монако (1992 г.), член Сербской академии наук (1997 г.), почетный член Американского колледжа хирургов (1998 г.), академик АМН Украины, почетный профессор МГУ им. М.В. Ломоносова (2011 г.), иностранный член Национальной Академии наук Грузии (2012 г.).
Он президент Ассоциации сердечно-сосудистых хирургов России (1995 г.), президент Общероссийской общественной организации «Лига здоровья нации» (2003 г.), член Общественной палаты РФ всех созывов.
Лечение ишемической болезни сердца
Лечение ишемической болезни сердца
Сердечная мышца нуждается в бесперебойном поступлении крови и кислорода.
- На частный приём ➝
- Прейскурант ➝
- По направлениям ➝
- Главная
- ➝
- На лечение
- ➝
- Лечение ишемической болезни сердца
Лечение ишемической болезни сердца
Сердечная мышца нуждается в бесперебойном поступлении крови и кислорода.
- На частный приём ➝
- Прейскурант ➝
- По направлениям ➝
Сердечная мышца нуждается в бесперебойном поступлении крови и кислорода. При ишемической болезни средца происходит стеноз коронарных артерий вследствие отложения липидных бляшек, что приводит к недостаточному снабжению сердечной мышцы кислородом и к появлению болевых ощущений.
Ишемическая болезнь способна вызывать боль в грудной клетке, прежде всего при физических нагрузках, но также и в состоянии покоя. Острая артериальная недостаточность может стать причиной инфаркта миокарда. Среди других возможных симптомов следует упомянуть усталость, одышку, нарушения сердечного ритма и сердечную недостаточность.
Для лечения ишемической болезни сердца в нашей клинике используются коронароангиография (CAG), измерение и баллонная ангиопластика стенозов (PCI) с использованием современных металлических стентов (BMS) и стентов с лекарственным покрытием (DES). При лечении также используется широкий спектр специальных технологий, таких как внутрисосудистое ультразвуковое исследование (IVUS), оптическая последовательная томография (OCT), метод определения резерва фракции потока (FFR), ротационная атерэктомия (ротабляция).
Выбор метода лечения
Порой одного медикаментозного лечения бывает недостаточно. Перед проведением инвазивных манипуляций всегда требуется выполнение коронароангиографии. Баллонная ангиопластика и стентирование коронарных артерий обычно позволяют добиться хорошего результата на начальном этапе лечения, а также при более легких формах заболевания. При тяжелых формах заболевания может применяться аортокоронарное шунтирование.
Выбор корректного метода лечения осуществляется на основании международных рекомендаций и опыта.
Принятию решения о хирургическом вмешательстве всегда предшествуют профессиональные консультации кардиолога и кардиохирурга. Помимо результатов коронароангиографии на выбор метода лечения влияют возможно имеющиеся фоновые заболевания (чаще всего это диабет, почечная недостаточность и заболевания легких), наличие сопутствующих заболеваний сердечно-сосудистой системы, возраст пациента, а также его личные пожелания относительно лечения.
Что такое коронароангиография?
Коронароангиография используется для диагностики ишемической болезни сердца. Она позволяет увидеть артерии на поверхности сердца, по которым в миокард доставляется кислород. Коронарных артерий две: правая и левая. Кроме того, от обеих артерий исходит множество ответвлений, и все их можно зафиксировать благодаря рентгеноконтрастному методу. Ишемическую болезнь сердца можно диагностировать в том случае, если в коронарных артериях будут обнаружены значительные сужения.
Когда стоит пройти коронароангиографию?
Вам следует пройти коронароангиографию, если вы испытываете сильную боль в грудной клетке или симптомы негативно влияют на качество вашей жизни, несмотря на адекватное медикаментозное лечение. Коронароангиография также показана, если во время клинического стресс-теста были замечены определенные проявления, которые указывают на тяжелую стадию ишемической болезни сердца. Если клинический стресс-тест и другие обследования не смогли объяснить происхождение болей в области грудной клетки, то в целях диагностики обоснованным является проведение коронароангиографии.
Как выполняется коронароангиография?
Коронароангиография проводится под местной анестезией, и пациент все время находится в сознании. Для выполнения процедуры кардиолог может выбрать вену на запястье или бедре. Через катетер, введенный в артерию, впрыскивается контрастное вещество и одновременно на рентгеновском аппарате делаются снимки артерий, заполненных контрастным веществом.
В большинстве случаев процедура может быть проведена амбулаторно, то есть пациент прибывает в Кардиоклинику утром и отправляется домой в тот же день после обследования. Иногда после коронароангиографии пациенту приходится провести одну ночь в больнице, если он принимает антикоагулянты или страдает от тяжелой почечной недостаточности.
Что такое баллонная ангиопластика и стентирование?
Ишемическая болезнь сердца развивается в результате стеноза коронарной артерии, доставляющей кислород в миокард. Стеноз может быть устранен с помощью баллонной ангиопластики или установки трубки из металлической сетки, так называемого стента (стентирование). Сначала суженную коронарную артерию расширяют с помощью баллонного катетера. Эту процедура называется баллонной ангиопластикой. Затем в место сужения вводится стент, который должен гарантировать, что артерия сохранится открытой.
Большая часть современных стентов покрывается лекарственными препаратами, поэтому речь идет о стентах с лекарственным покрытием. Лекарственное покрытие активно препятствует повторному образованию стеноза на прежнем месте после окончания процедуры. Кардиолог оценивает в каждом отдельном случае, какой стент следует использовать — обычный или с лекарственным покрытием.
В каких случаях проводятся баллонная ангиопластика и стентирование?
Баллонная ангиопластика применяется к тем участкам, где во время коронароангиографии были замечены значимые стенозы. При рассмотрении вопроса о применении ангиопластики и стентирования основное значение имеет симптоматика пациента. В неоднозначных ситуациях при оценке клинического значения стеноза в качестве вспомогательного средства можно использовать результаты клинического стресс-теста и дополнительные исследования, сопутствующие коронароангиографии.
К ним относятся внутрисосудистое ультразвуковое исследование коронарной артерии (IVUS) и оптическая последовательная томография (OCT). С их помощью можно составить точную картину о степени стеноза. Также значимость стеноза для кровообращения миокарда можно проверить непосредственно во время коронароангиографии (FFR, метод определения резерва фракции потока).
На основании полученных результатов в каждом отдельном случае выбирается наилучший метод лечения, которым может быть прием оптимального лекарственного препарата, баллонная ангиопластика или аортокоронарное шунтирование.
Как процедура проходит на практике?
Баллонная ангиопластика и стентирование проводятся под местной анестезией, и пациент все время находится в сознании. Для выполнения процедуры кардиолог может выбрать вену на запястье или бедре.
С помощью катетера, введенного в коронарную артерию, через место сужения протягивается тонкий тросик. Сначала с помощью этого тросика осуществляется баллонная ангиопластика, а затем стентирование.
В большинстве случаев ангиопластика и стентирование могут быть проведены амбулаторно, то есть пациент прибывает в Кардиоклинику утром и отправляется домой в тот же день после проведения процедуры. Иногда после процедуры пациенту приходится провести одну ночь в больнице, если он принимает антикоагулянты или страдает от тяжелой почечной недостаточности.
В настоящее время в большинстве случаев баллонная ангиопластика проводится в связи с коронароангиографией, поэтому для проведения ангиопластики отдельный визит не требуется. Смотреть видео об опыте пациента: Коронароангиография и баллонная ангиопластика.
Как проходит операция аортокоронарного шунтирования?
До операции пациент проходит премедикацию. Уже в операционной выполняются подготовительные мероприятия и производится общая анестезия, при которой пациент погружается в состояние сна. Чаще всего для шунтирования посередине грудной клетки выполняется продольный разрез. Операция выполняется на остановленном сердце, что делает возможной работу на неподвижном, бескровном операционном поле.
Пациента подключают к аппарату искусственного кровообращения, с помощью которого отсасываемая из организма кровь обогащается кислородом и направляется обратно в систему кровообращения. Таким образом, аппарат искусственного кровообращения выполняет функции сердца и легких в среднем в течение целого часа. С помощью тончайшей атравматической нити аутовенозный шунт подшивается через разрез длиной несколько миллиметров, выполненный на ветви коронарной артерии ниже уровня сужения. Участки, пораженные окклюзией или стенозом, как правило, не удаляются. В качестве шунтов применяются внутренние грудные артерии (доступ к ним обеспечивает продольный разрез грудной клетки), лучевая артерия из предплечья или артерии нижних конечностей.
Операция аортокоронарного шунтирования может при необходимости также выполняться без остановки сердца и использования аппарата искусственного кровообращения. В этом случае операция от начала до конца проводится на «работающем» сердце. Для стабилизации коронарных артерий, расположенных на поверхности сердца, на участок с шунтируемой коронарной артерией накладывается специальное стабилизирующее устройство, что позволяет выполнить вшивание шунта.
При операции на бъющемся сердце необязательно задействовать главную аорту, что позволяет сократить риски острого нарушения мозгового кровообращения у пациентов с атеросклерозом восходящей аорты или кровеносных сосудов головного мозга, у которых кроме того ранее уже могли наблюдаться окклюзии сосудов головного мозга. Техника шунтирования на бъющемся сердце может оказаться предпочтительной также в случаях, когда пациент страдает заболеванием легких или почечной недостаточностью.
Что происходит после операции?
В среднем послеоперационное лечение в Кардиоклинике занимает от 4 до 6 суток, и примерно столько же дней пациент проходит восстановительную терапию в больнице. Заживление грудной клетки происходит в течение 6–8 недель, и пациенту может быть назначен больничный продолжительностью 2–3 месяца. Чаще всего операция проводится с целью улучшения качества жизни и повышения функциональных способностей организма, в некоторых случаях она также может быть необходима для предотвращения серьезного приступа болезни.
В дальнейшем, чтобы надолго сохранить положительный эффект от операции, важно держать под контролем факторы риска, приведшие к ишемической болезни, поскольку высокое артериальное давление, повышенный уровень холестерина и диабет будут влиять также и на проходимость трансплантированного сосуда. Необходим регулярный мониторинг.