Симптомы и лечение тромбоза нижней верхней полой вены
Симптомы и лечение тромбоза нижней верхней полой вены

Флеботромбозы нижних конечностей – одна из ведущих по клинической и научной значимости проблем практической флебологии [1]. Они широко распространены среди взрослого населения, а медикаментозное лечение недостаточно эффективно. При этом сохраняется высокий уровень нетрудоспособности и инвалидности [2, 3]. Отличает флеботромбозы стертость клинической картины в первые часы и дни заболевания, а первым симптомом становится легочная тромбоэмболия (ТЭЛА), являющаяся ведущей причиной как общей, так и хиругической летальности [1]. В связи с этим предельно важна своевременная и точная диагностика эмболоопасных венозных тромбозов с использованием информативных, доступных и неинвазивных способов [4–6]. Ультразвуковое доплеровское сканирование (УЗДС) стало основным методом диагностики указанных флеботромбозов, являющихся потенциальным источником развития легочной тромбоэмболии [1, 4, 7].
В литературе [7, 8] немного публикаций, в которых подробно освещаются ультразвуковые характеристики эмбологенности венозного тромба. Ведущими критериями эмбологенности тромба считаются степень его подвижности и длина и эхогенность флотирующей части, характеристика внешнего контура тромба (ровный, неровный, нечеткий), наличие циркулярного потока крови вокруг тромба в режиме цветового дуплексного картирования как при продольном, так и поперечном сканировании [8–12].
Профилактика ТЭЛА является неотъемлемым компонентом лечения больных с острым венозным тромбозом [13]. К сожалению, использование непрямых антикоагулянтов не способствует профилактике отрыва и миграции в легочные артерии сформированных тромбов [11]. Поэтому при выявлении протяженного флотирующего и эмболоопасного тромбоза показано хирургическое вмешательство, направленное на предотвращение миграции тромбоэмбола (тромбэктомия, пликация или эндоваскулярная имплантация кава-фильтра) [3–6, 14–17].
Вопрос о хирургической тактике при флотирующем тромбозе глубоких вен конечностей должен решаться индивидуально с учетом локализации проксимальной части тромба, её протяженности, флотации, наличия коморбидной и интеркуррентной патологии [9–11, 16–19].
При наличии тяжелой интеркуррентной патологии и противопоказаний к выполнению открытой операции у больных с эмболоопасными тромбозами магистральных вен показана установка кава-фильтра по абсолютным показаниям (противопоказания к антикоагулянтной терапии, эмболоопасные тромбозы при невозможности выполнения хирургической тромбэктомии, рецидивирующие ТЭЛА) [20, 21]. При этом важно учитывать факт фиксации флотирующих тромбов (длина тромба не более 2 см) и возможность консервативной тактики лечения [9–11, 18, 22–24].
Непредсказуемость течения венозных тромбозов в системе нижней полой вены доказывается дигностикой флотирующих тромбозов у пациентов без каких-либо клинических признаков венозной патологии, обнаружением эмболоопасных тромбозов у больных с хроническими заболеваниями вен, факты тромбоэмболий легочной артерии при окклюзирующих формах тромбозов глубоких вен [25, 26].
Цель исследования: улучшение сонографической диагностики и результатов ургентных вмешательств у больных с острыми флеботромбозами.
Материалы и методы исследования
Нами проанализированы результаты физикальной и сонографической диагностики флеботромбозов нижних конечностей у 334 пациентов, находившихся на стационарном лечении в государственном бюджетном учреждении здравоохранения Республики Мордовия «Республиканская клиническая больница № 4». Возраст пациентов составил 20–81 лет; 52,4 % составили женщины, 47,6 % – мужчины; 57,0 % из них были трудоспособного, а 19,4 % – молодого возраста (табл. 1).
Пол и возраст обследованных больных
61 год и старше
Распределение флотирующих тромбов в системе глубоких вен нижних конечностей
Глубокие вены бедра
Подколенная вена и вены голени
Подкожные вены бедра
Самой большой оказалась группа пациентов от 61 года и старше (143 человека), среди мужчин преобладали лица в возрасте от 46 до 60 лет – 66 (52,3 %) человек, у женщин – в возрасте 61 года и старше – соответственно 89 (62,3 %) человек.
Флеботромбозы у мужчин в возрасте до 45 лет чаще встречались у лиц, злоупотребляющих внутривенным введением психоактивных веществ. В возрасте 60 лет и более число больных женского пола начинает преобладать над мужским, что объясняется преобладанием у женщин иных факторов риска: гинекологические заболевания (миома матки больших размеров, опухоли яичников), ИБС, ожирение, травмы, варикозное расширение вен и другие. Снижение заболеваемости в общей популяции у мужчин в возрасте 60 лет и более объясняется снижением их доли в соответствующих возрастных группах, высокой летальностью от ТЭЛА, развитием хронической венозной недостаточности и посттромбофлебитического синдрома.
Ультрасонографическая диагностика и эхоскопический мониторинг проводились на ультразвуковых аппаратах Vivid 7 (General Electric, США), Toshiba Aplio, Toshiba Xario (Япония), работающих в режиме реального времени с использованием конвексных датчиков 2–5, 4–6 МГц и линейных датчиков с частотой 5–12 МГц. Исследование начинали с проекции бедренной артерии (в паховой области) с оценки кровотока в поперечном и продольном сечении по отношению к продольной оси вены. При этом оценивали кровоток бедренной артерии. При сканировании оценивались диаметр вены, ее сжимаемость (путем компрессии вены датчиком до прекращения кровотока при сохранении кровотока в артерии), состояние просвета, сохранность клапанного аппарата, наличие изменений на стенках, состояние паравазальных тканей. Состояние гемодинамики вен оценивалось с использованием функциональных проб: дыхательной и кашлевой пробы или пробы с натуживанием. При этом оценивалось состояние вен бедра, подколенной вены, вен голени, а также большой и малой подкожных вен. Оценку гемодинамики нижней полой вены, а также подвздошных, большой подкожной, бедренных вен и вен голени в дистальном отделе проводили в положении пациента лежа на спине. Исследование же подколенных вен, вен верхней трети голени и малой подкожной вены проводилось в положении пациента лежа на животе с валиком, подложенным под область голеностопных суставов. Для исследования магистральных вен и при затруднениях в исследовании использовался конвексный, в остальном – линейные датчики.
Сканирование в поперечном сечении проводили для выявления подвижности головки тромба, о чем свидетельствовало полное соприкосновение венозных стенок при незначительной компрессии датчиком. В ходе обследования устанавливался характер флеботромбоза: пристеночный, окклюзионный или флотирующий.
В перечень лабораторных методов диагностики входили определение уровня Д-димера, коагулограмма, исследование маркеров тромбофилии. При подозрении на перенесенную ТЭЛА в комплекс обследования также входила компьютерная томография в режиме ангиопульмонографии и исследование брюшной полости и малого таза.
С целью хирургической профилактики ТЭЛА при острых флеботромбозах были использованы 3 способа операции: имплантация кава-фильтра, пликация сегмента вены и кроссэктомия и/или флебэктомия. В послеоперационном периоде ультразвуковая диагностика преследовала цель оценки состояния венозной гемодинамики, степени реканализации или усиления тромботического процесса в венозной системе, наличия или отсутствия фрагментации тромба, наличия флотации, тромбоза вен контралатеральной конечности, тромбоза зоны пликации или кава-фильтра и определялись линейная и объемная скорости кровотока и коллатеральный кровоток.
Cтатистический анализ производили с помощью программы Statistica. Оценка различий результатов между группами проведена по критериям Пирсона (проведена по критериям Пирсона) и Стьюдента (t). Статистически достоверными считались различия, уровень значимости которых был более 95 % (р
Тромбоз глубоких вен нижних конечностей
Говоря о здоровье сосудов, обязательно следует упомянуть о таком коварном заболевании, как тромбоз глубоких вен. Коварного – поскольку от своевременного обращения к врачу и правильного лечения зависит не только качество жизни пациента, но и сама жизнь. Причин тромбоза три: повышение свертываемости крови, замедление кровотока в вене, повреждение сосудистой стенки. К факторам риска тромбоза относятся врожденные (генетические) или приобретенные заболевания свертывающей системы крови, онкологические заболевания, прием некоторых препаратов, в частности, гормональных, преклонный возраст, избыточный вес, обширные операции, переломы, тяжелые травмы и заболевания центральной нервной системы, курение. К сожалению, даже при имеющимся широком диагностическом арсенале не всегда возможно установить причину тромбоза. Многие механизмы тромбообразования до сих пор остаются не известными современной медицинской науке. Наиболее распространенной и опасной локализацией тромбоза являются глубокие вены нижних конечностей.
Залогом успешного лечения данной патологии является ранняя диагностика и лечение. Для этого необходимо знать симптомы заболевания. Самым частым из них является отек. В зависимости от локализации тромбоза может отекать лодыжка, голень или все бедро, отек, как правило, равномерный, плотный, часто сопровождается изменением цвета кожи. К симптомам венозного тромбоза так же могут относиться боль в икроножной мышце, тяжесть в ногах, судороги, однако эти симптомы не специфичны. В редких случаях тромбоз глубоких вен проходит без симптомов и сразу приводит к такому осложнению как тромбоэмболия легочной артерии — отрыву и попаданию фрагмента тромба в легочную артерию, закупорка которой может привести к летальному исходу. Симптомами легочной тромбоэмболии являются боль в грудной клетке, кровохарканье, сердцебиение, при тяжелом поражении одышка, синюшность верхней половины тела, потеря сознания.

Основным методом диагностики венозного тромбоза является ультразвуковое исследование вен, которое в большинстве случаев позволяет установить распространенность тромбоза, а так же наличие и отсутствие подвижности тромба — флотацию. Вовремя начатая медикаментозная терапия венозного тромбоза препаратами, снижающими свертываемость крови, антикоагулянтами, а так же использование компрессионной терапии (ношение специальных чулок и гольфов увеличивающих отток крови) приводит к успешному излечению тромбоза и предотвращению легочной тромбоэмболии без операции. У части пациентов может развиться так называемый посттромбофлебитических синдром в результате повреждения тромбами венозной стенки или сохранения закупорки вен после лечения, что в последующем требует длительной или пожизненной компрессионной терапии.
Хирургическое лечение тромбоза используется в исключительных случаях, даже при наличии подвижного (флотирующего) тромба. Хирургическое удаления тромба из вен или тромбэктомия, возможна только в единичных случаях, показания к такой операции строго ограничены. Использование тромбэктомии у всех пациентов просто не приведёт к успеху и может быть опасным для пациента. Другим хирургическим методом лечения тромбоза является имплантация кава — фильтра. Кава — фильтром называют специальную ловушку, которая устанавливается в самую крупную вену нашего организма — нижнюю полую — и препятствует попаданию тромба и его фрагментов в лёгочные артерии. Используется данная методика только в случае высокого риска отрыва тромба с развитием легочной тромбоэмболии, когда длина его подвижной части достигает 7см и более, а так же при невозможности или неэффективности лечения препаратами, снижающими свертываемость крови.
Государственное бюджетное учреждение здравоохранения «Тамбовская областная больница имени В.Д. Бабенко» единственное учреждение, в котором имеется отделение сосудистой хирургии. При обследовании больных применяется весь арсенал современных методов диагностики данной патологии, в том числе ультразвуковое дуплексное сканирование вен, контрастная флебография, компьютерная ангиография легочных артерий, крупных магистральных вен грудной клетки и брюшной полости. При обращении пациента на основании проведенных исследований делается заключение о возможности лечения данной патологии хирургически или медикаментозно, а так же амбулаторно или в стационаре. Высококвалифицированные врачи успешно используют современные методы лечения, как консервативные, так и хирургические (тромбэктомия из магистральных вен, имплантация кава — фильтра, тромболизис).
5.3. Лечебная тактика при тромбозе глубоких вен
- ← 5.2. Клиническая картина и диагностика тромбоза глубоких вен
- Содержание
- → 5.4. Диагностика тромбоэмболии легочных артерий
Постельный режим и возвышенное положение конечности может уменьшить болевой синдром, однако строгий постельный режим существенно не влияет на частоту развития ТЭЛА, при условии что верифицированный тромбоз не является флотирующим. Более того, болевой синдром и отек уменьшаются гораздо быстрее при ранней активизации и адекватной компрессии нижних конечностей с помощью специализированного компрессионного трикотажа 2—3-го класса. Когда отек нестабилен (т. е. объем конечности имеет значительную суточную динамику), допустимо использование эластичных бинтов длинной растяжимости.
Неоспорима необходимость адекватной антикоагулянтной терапии как основы лечения больных с ТГВ (в том числе бессимптомного). Антикоагулянтная терапия НФГ или НМГ при обоснованном подозрении на ТГВ может быть начата до инструментальной верификации диагноза.
1. Внутривенно болюсом 80 МЕ/кг (или 5000 МЕ) и инфу зия с начальной скоростью 18 МЕ/кг в 1 ч (или 1250— 1300 МЕ/ч), затем подбор дозы МЕ по значениям АЧТВ. Цель — поддержка АЧТВ в 1,5—2,5 раза выше верхней границы нормы для конкретной лаборатории.
1. Подкожно 100 анти-Ха МЕ (1 мг)/кг 2 раза в сутки
2. Подкожно 150 анти-Ха МЕ (1,5 мг)/кг 1 раз в сутки
Фрагмин (Далтепарин) 1. Подкожно 100 анти-Ха МЕ/кг 2 раза в сутки
2. Подкожно 200 анти-Ха МЕ/кг (максимально 18 000 МЕ) 1 раз в сутки
1. Подкожно 86 анти-Ха МЕ/кг 2 раза в сутки
2. Подкожно 172 анти-Ха МЕ/кг (максимально 17 100 МЕ) 1 раз в сутки
В начале становления флебологии как отдельной хирургической специальности одним из главных вопросов, требующих незамедлительного решения, был вопрос профилактики ТЭЛА при флеботромбозах. После разработки в 1959 г. метода внешней пликации полой вены матрацными швами и внешней пликации клеммами удалось определить дальнейшее направление решения проблемы острых глубоких флеботромбозов и их осложнения — ТЭЛА. До 1967 г. метод, в сочетании с консервативной терапией, оставался единственным клиническим подходом в данной проблеме. Несмотря на то что выполнение технологии внешнего парциального клипирования клеммами сопряжено с необходимостью травматичного хирургического доступа и практически невыполнимо у тяжелобольных пациентов, данный подход в ограниченных ситуациях применяется и совершенствуется до настоящего времени (например, с использованием эндовидеоскопической техники). Созданный и примененный клинически в 1967 г. внутрипросветный зонтичный кава-фильтр Моббина—Аддина явился первым опытом подобного эндоваскулярного вмешательства. Дальнейшее развитие данного направления велось преимущественно по пути совершенствования конструкции кавафильтров и изучения их влияния на гемодинамику и клиническое течение основного процесса. Показаниями к имплантации кава-фильтра являются невозможность проведения и неэффективность адекватной антикоагулянтной терапии, флотирующий тромб с узким основанием, невозможность его удаления оперативно, рецидивирующая ТЭЛА у больных с высокой легочной гипертензией.
У молодых пациентов при устранимых факторах риска и причинах ТГВ необходимо имплантировать съемные модели, которые удаляют в срок до 30 сут после установки при устранении угрозы ТЭЛА.
Уже неоднократно отмечено, что в результате установки кава-фильтров в ближайшем периоде с частотой 1,5—8% могут возникать ТЭЛА, а в сроки до 3 лет с частотой 12—25% возникает тромбоз нижней полой вены.
В основе посттромботической болезни лежит затруднение венозного оттока, которое приводит к патофизиологическим изменениям, характерным для хронической венозной недостаточности: отеку, гиперпигментации и липодерматосклерозу. Именно нарушение венозного оттока, вызванное обструкцией, приводит к наиболее тяжелым формам посттромботической болезни. Таким образом, лечебная тактика, направленная на удаление тромба, является патофизиологически обоснованной и в значительной степени снижает риск тяжелой посттромботической болезни.

После завершения тромбэктомии из илеофеморального сегмента интраоперационно следует выполнить флебографию/ -скопию для оценки проходимости подвздошных вен. В качестве дополнительного высокоинформативного метода интраоперационного контроля можно использовать внутрисосудистое УЗИ.
Уровень тромбоза ниже общей подвздошной вены позволяет проводить вмешательство без введения в просвет вены катетеров и других травмирующих инструментов.
Принципиально решение проблемы хирургической тромбэктомии из бедренно-подколенного сегмента сегодня рассматривается в двух направлениях: решение вопроса методом переключения флебогемодинамики на глубокую бедренную вену и путем восстановления естественного потока с возможным сохранением клапанного аппарата собственно бедренной и/или подколенной вен. Если наличие эмбологенного тромба в сегменте можно считать абсолютным показанием к активной тактике, то при обтурирующих тромбах вопрос решается с учетом давности процесса. Известно, что эффективная тромбэктомия возможна только при тромбах давностью не более 3—7 сут [Савельев В. С., 2001]. Существует расхожее мнение о том, что следует придерживается осторожной тактики при хирургическом удалении тромбомасс из бедренно-подколенного сегмента, завершая операцию перевязкой или резекцией приустьевого сегмента собственно бедренной вены, оценивая ближайшие результаты как хорошие по отсутствию симптомов хронической венозной недостаточности. Расчет при таком подходе ведется на переключение основного венозного потока на глубокую вену бедра, которая и должна обеспечить устойчивый отток. Однако известно, что последняя только в 38% случаев имеет прямую связь с подколенной веной [Mavor G. E., Galloway J. M., 1967].
Именно поэтому предложен способ тромбэктомии при лечении эмбологенного флеботромбоза, направленный не только на удаление тромба, но и на сохранение бедренной вены как полноценного органа, включая систему клапанов.
Показано [Кайдорин А. Г., Цыплящук А. В., 2008], что циркулярное выделение вены приводит к выраженному нарушению интрамурального кровообращения и, как следствие, рубцовым изменениям в стенке, клапанной деформации.
Поэтому в ходе доступа из перивенозных тканей выделяется только передневнутренняя стенка вены на протяжении 1— 2 см, по возможности повреждая адвентицию только по линии разреза и не более чем на 1/2 окружности.
На 1—1,5 см выше проекции основания флотирующей части тромба и обязательно выше проксимального клапана бедренной вены в поперечном направлении накладываются П-образные швы-держалки монофиламентной нитью 6/0, между которыми поперечно производится вскрытие просвета вены.
Флотирующая часть тромба при повышении внутрибрюшного давления (натуживании пациента) самопроизвольно вывихивается в рану под давлением обратного тока крови. После получения ретроградного кровотока свободную вену выше места инцизии прижимают мягким тупфером или пальцем.
При адекватном размере флеботомического отверстия, в ряде случаев, выведенный тромб может служить временным тампоном, препятствующим истечению крови в рану.
Затем при помощи интенсивной поступательной компрессии мягких тканей голени и бедра удаляют тромбы из дистальных глубоких вен нижней конечности.
При невозможности полного удаления тромбомасс на всем протяжении вены в обязательном порядке необходимо убедиться и оценить качество антеградного потока через ПКБВ. Последнее необходимо для оценки перспективы сохранения функции клапана. Если добиться антеградного кровотока не удается, а стенка бедренной вены в зоне операции подвержена воспалительным или рубцово-склеротическим изменениям, следует выполнить ее перевязку ниже впадения глубокой бедренной вены, так как высока вероятность ретромбоза.
При адекватном антеградном кровотоке, убедившись в отсутствии подвижных частей тромба, П-образные швы подтягивают, при этом образуется клапаноподобная дубликатура, обеспечивающая временный гемостаз. Также временный гемостаз легко осуществляется пальцевым прижатием выше и ниже флеботомического дефекта (через массу перивазальных тканей.
В послеоперационном периоде продолжается парентеральное введение антикоагулянтов. Параллельно подбирают дозу оральных антикоагулянтов до достижения целевого значения МНО (2,0—3,0)
Синдром верхней полой вены ( Кава-синдром , СВПВ )
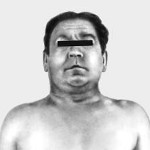
Синдром верхней полой вены – это симптомокомплекс, развивающийся вследствие нарушения кровообращения в системе верхней полой вены и затруднения оттока венозной крови от верхних отделов туловища. Классическими признаками синдрома верхней полой вены служат: цианоз; одутловатость головы, шеи, верхних конечностей, верхней половины грудной клетки; расширение подкожных вен; одышка, охриплость голоса, кашель и др. Нередко развиваются общемозговые, глазные, геморрагические проявления. Диагностический алгоритм может включать проведение рентгенографии ОГК, венокаваграфии, КТ и МРТ грудной клетки, УЗДГ, медиастиноскопии, торакоскопии с биопсией. При синдроме может быть предпринята эндоваскулярная баллонная ангиопластика и стентирование, тромбэктомия, резекция ВПВ, обходное шунтирование, паллиативное удаление опухоли с целью декомпрессии средостения.
МКБ-10

- Причины СВПВ
- Симптомы СВПВ
- Осложнения
- Диагностика
- Лечение СВПВ
- Прогноз
- Цены на лечение
Общие сведения
Под синдромом верхней полой вены (СВПВ), или кава-синдромом, понимают вторичное патологическое состояние, осложняющее многие заболевания, связанные с поражением органов средостения. В основе кава-синдрома лежит экстравазальная компрессия или тромбоз верхней полой вены, нарушающие отток венозной крови от головы, плечевого пояса и верхней половины туловища, что может приводить к жизнеугрожающим осложнениям. Синдром верхней полой вены в 3-4 раза чаще развивается у пациентов мужского пола в возрасте 30-60 лет. В клинической практике с синдромом верхней полой вены приходится сталкиваться специалистам в области торакальной хирургии и пульмонологии, онкологии, кардиохирургии, флебологии.
Верхняя полая вена (ВПВ) располагается в среднем средостении. Она представляет собой тонкостенный сосуд, окруженный плотными структурами — грудной стенкой, аортой, трахеей, бронхами, цепочкой лимфоузлов. Особенности строения и топографии ВПВ, а также физиологически низкое венозное давление обусловливают легкое возникновение обструкции магистрального сосуда. Через ВПВ оттекает кровь от головы, шеи, верхнего плечевого пояса и верхних отделов грудной клетки. Верхняя полая вена имеет систему анастомозов, выполняющих компенсаторную функцию при нарушении проходимости ВПВ. Однако венозные коллатерали не могут полностью заменить ВПВ. При синдроме верхней полой вены давление в ее бассейне может достигать 200-500 мм вод. ст.

Причины СВПВ
Развитию синдрома верхней полой вены могут способствовать следующие патологические процессы: экстравазальная компрессия ВПВ, опухолевая инвазия стенки ВПВ или тромбоз. В 80-90% случаев непосредственными причинами кава-синдрома выступают рак легкого, преимущественно правосторонней локализации (мелкоклеточный, плоскоклеточный, аденокарцинома); лимфогранулематоз, лимфомы; метастазы рака молочной железы, рака простаты и рака яичка в средостение; саркома и др.
В остальных случаях к компрессии ВПВ могут приводить доброкачественные опухоли средостения (кисты, тимомы), фиброзный медиастинит, аневризма аорты, констриктивный перикардит, инфекционные поражения: (сифилис, туберкулез, гистоплазмоз), загрудинный зоб. Синдром верхней полой вены может быть обусловлен тромбозом ВПВ, развивающимся на фоне длительной катетеризации вены центральным венозным катетером или пребывания в ней электродов электрокардиостимулятора.
Симптомы СВПВ
Клинические проявления синдрома верхней полой вены обусловлены повышением венозного давления в сосудах, кровь от которых в норме оттекает через ВПВ или безымянные вены. На выраженность проявлений влияют скорость развития синдрома верхней полой вены, уровень и степень нарушения кровообращения, адекватность коллатерального венозного оттока. В зависимости от этого клиническое течение синдром верхней полой вены может быть медленно прогрессирующим (при компрессии и инвазии ВПВ) или острым (при тромбозе ВПВ).
Классическая триада, характеризующая синдром верхней полой вены, включает отек, цианоз и расширение поверхностных вен на лице, шее, верхних конечностях и верхней половине туловища. Пациентов может беспокоить одышка в покое, приступы удушья, охриплость голоса, дисфагия, кашель, боли в груди. Указанные симптомы усиливаются в положении лежа, поэтому больные вынуждены принимать в постели полусидячее положение. В трети случаев отмечается стридор, обусловленный отеком гортани и угрожающий обструкцией дыхательных путей.
Осложнения
Часто при синдроме верхней полой вены развиваются носовые, легочные, пищеводные кровотечения, вызванные венозной гипертензией и разрывом истонченных стенок сосудов.
Нарушение венозного оттока из полости черепа приводит к развитию церебральных симптомов:
- головной боли
- шума в голове
- сонливости
- судорог
- спутанности и потери сознания.
В связи с нарушением функции глазодвигательных и слуховых нервов могут развиваться:
- диплопия
- двусторонний экзофтальм
- слезотечение
- утомляемость глаз
- снижение остроты зрения
- тугоухость
- слуховые галлюцинации
- шум в ушах
Диагностика
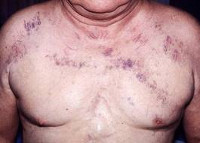
Физикальное обследование пациента с синдромом верхней полой вены выявляет набухание вен шеи, расширенную сеть подкожных венозных сосудов на груди, полнокровие или цианоз лица, отек верхней половины туловища. При подозрении на синдром верхней полой вены всем больным показано рентгенологическое обследование — рентгенография грудной клетки в двух проекциях, томография (компьютерная, спиральная, магнитно-резонансная). В некоторых случаях для определения локализации и выраженности венозной обструкции прибегают к проведению флебографии (венокаваграфии).

С целью дифференциальной диагностики тромбоза ВПВ и обструкции извне показана УЗДГ сонных и надключичных вен. Осмотр глазного дна офтальмологом позволяет выявить извитость и расширение вен сетчатки, отек перипапиллярной области, застойный диск зрительного нерва. При измерении внутриглазного давления может отмечаться его значительное повышение.
Для определения причин синдрома верхней полой вены и верификации морфологического диагноза может потребоваться проведение бронхоскопии с биопсией и забором мокроты; анализа мокроты на атипичные клетки, цитологического исследования промывных вод из бронхов, биопсии лимфатического узла (прескаленной биопсии), стернальной пункции с исследованием миелограммы. При необходимости может выполняться диагностическая торакоскопия, медиастиноскопия, медиастинотомия или парастернальная торакотомия для ревизии и биопсии средостения.
Дифференциальную диагностику кава-синдрома проводят с застойной сердечной недостаточностью: при синдроме верхней полой вены отсутствуют периферические отеки, гидроторакс, асцит.
Лечение СВПВ
Симптоматическое лечение синдрома верхней полой вены направлено на повышение функциональных резервов организма. Оно включает назначение низкосолевой диеты, ингаляций кислорода, диуретиков, глюкокортикоидов. После установления причины, вызвавшей развитие синдрома верхней полой вены, переходят патогенетическому лечению.
Так, при синдроме верхней полой вены, обусловленном раком легкого, лимфомой, лимфогранулематозом, метастазами опухолей других локализаций, проводится полихимиотерапия и лучевая терапия. Если развитие синдрома верхней полой вены вызвано тромбозом ВПВ, назначается тромболитическая терапия, проводится тромбэктомия, в некоторых случаях – резекция сегмента верхней полой вены с замещением резецированного участка венозным гомотрансплантатом.
При экстравазальной компрессии ВПВ радикальные вмешательства могут включать расширенное удаление опухоли средостения, удаление медиастинальной лимфомы, торакоскопическое удаление доброкачественной опухоли средостения, удаление кисты средостения и др. В случае невозможности выполнения радикальной операции прибегают к различным паллиативным хирургическим вмешательствам, направленным на улучшение венозного оттока: удалению опухоли средостения с целью декомпрессии, обходному шунтированию, чрескожной эндоваскулярной баллонной ангиопластике и стентированию верхней полой вены.
Прогноз
Отдаленные результаты лечения синдрома верхней полой вены зависят, прежде всего, от основного заболевания и возможностей его радикального лечения. Устранение причин приводит к купированию проявлений кава-синдрома. Острое течение синдрома верхней полой вены может вызвать быструю гибель больного. При синдроме верхней полой вены, обусловленном запущенным онкологическим процессом, прогноз неблагоприятный.
Синдром верхней полой вены
Клиническая картина синдрома верхней полой вены (СВПВ) очень показательна при выраженном блоке венозного оттока. Как правило, главный признак — выраженная отёчность головы и шеи с синюшным оттенком за счёт просвечивания через кожу «тёмной» венозной крови. Шея настолько сильно отекает, что её почти нет. Набрякшие веки и раздутые губы, на лице и шее контурируются и выбухают расширенные вены. Руки отекают несильно, поскольку сокращения мышц «выдавливают» кровь из мелких вен в центровой сосуд.
Пациент жалуется на головные боли и шум в голове, что объясняется отёком. Давление в головном мозге у ранее здорового человека должно оставаться в норме, за этим следит специфический гематоэнцефалический барьер (ГЭБ). У пожилых людей, а также при сопутствующих сердечно-сосудистых заболеваниях и диабете функция ГЭБ страдает, поэтому внутричерепное давление может повыситься. Проявляется это и скачками артериального давления — кризами, и потерей сознания, и сонливостью, и судорогами.
Может определяться небольшая отёчность передней грудной стенки в верхних отделах — надключичной и подключичной областях. Небольшой диффузный отёк называют пастозностью, при ней надавливание на кожу оставляет небольшое вдавление. Отекают голосовые связки, и голос меняется на негритянский тембр — как бы «толстый» и осиплый. Из-за застоя в лёгких возникают кашель, одышка. За счёт отёка глотки и пищевода беспокоит ощущение нарушения проходимости твёрдой пищи — дисфагия. Возникает чувство распирания груди изнутри.
Симптомы синдрома верхней полой вены
В зависимости от причины синдрома, симптоматика может развиваться медленно или быстро. Быстро — при агрессивных опухолях, таких как злокачественная лимфома и мелкоклеточный рак лёгкого. Постепенно проявляются клинические признаки при метастазах в лимфатические узлы рака и венозный тромбоз. Выраженность признаков синдрома верхней полой вены зависит от уровня, на котором частично перекрывается вена и степени сужения её просвета.
При любой скорости развития синдрома верхней полой вены наступает тот момент, когда без экстренной медицинской помощи обойтись невозможно.
До середины прошлого века синдром верхней полой вены (СВПВ), а если быть точным, то синдром её сдавления, вызывал только третичный сифилис, когда гуммы разрушали стенку грудной аорты с формированием аневризматических мешков, сдавливавших органы средостения и верхнюю полую вену в том числе. Третичный сифилис искоренили антибиотиками, но с начала ХХ века распространилось курение, а с ним и тысячекратно выросла заболеваемость раком лёгкого, который и стал основной причиной неотложного состояния, вызванного нарушением кровообращения очень крупной вены и впадающих в неё сосудов.
Сколько людей ежегодно настигает СВПВ, точно неизвестно, медицинская статистика учитывает только этиологическую причину — рак лёгкого, но не его осложнения, тем не менее, в последние годы пациенты с СВПВ всё чаще попадают в онкологическую реанимацию по причине критичной для жизни тяжести состояния. Большинство всех диагностированных СВПВ обусловлены распространённым раком лёгкого, причём восемь случаев из десяти вызваны опухолью правого лёгкого. Если разбираться с морфологией, то преимущественно венозный синдром инициирует мелкоклеточный рак лёгкого, реже плоскоклеточный, и совсем редко аденокарцинома. Два последних относят к немелкоклеточному раку лёгкого.
На втором месте по частоте индукции СВПВ стоят онкогематологические заболевания — высокозлокачественные лимфомы или лимфосаркомы, поражающие переднее средостение, чаще лимфобластные и диффузные крупноклеточные. Как правило, это очень агрессивные, растущие буквально за несколько дней опухоли. Синдром развивается при метастазах в лимфоузлах средостения любого рака, но чаще это органы, лимфоколлекторы которых находятся в средостенной клетчатке: молочная железа, пищевод и желудок. Метастазы герминогенных опухолей яичка распространяются от забрюшинных до надключичных зон преимущественно по лимфатическим путям, но на их долю приходится немного случаев СВПВ.
Почему так происходит?
Полые вены впадают в правые отделы сердца: предсердие и желудочек. При расслаблении правого предсердия в него под небольшим давлением подаётся почти бескислородная венозная кровь. Из предсердия кровь идёт в правый желудочек, откуда она выжмется в лёгочную артерию, чтобы в альвеолах лёгких насытиться кислородом и по лёгочным венам вернуться в сердце, но в левые отделы, которые через аорту погонят обогащённую кислородом питательную жидкость ко всем органам.
Нижняя полая вена собирает «отработанную» кровь от всех органов ниже диафрагмы. Верхняя полая вена — от органов, расположенных выше диафрагмы. Бассейны обеих вен чётко разграничены, определённые сосудистые веточки несут кровь в верхнюю полую, другие — строго в нижнюю, но есть и сосудистые сообщения между «верхними» и «нижними», называемые анастомозы. При сужении просвета верхней полой вены, частично эти анастомозы сбрасывают избыток крови через ветви, идущие к нижней полой вене.
Верхняя полая вена тонкостенная, её мышечная оболочка — одно название, венозная кровь от головы и шеи идёт практически под давлением силы тяжести, движению помогают развитые мышцы рук и плечевого пояса. Рядом с веной в средостении проходят мощная аорта, где огромное давление крови, состоящие из хрящевых колец трахея и бронхи, и стелются цепочки лимфатических узлов, откачивающие лимфу от лёгких и других ближайших органов. Вот эти цепочки и создают проблемы, когда в них развиваются метастазы. Если аорта может противостоять сдавлению извне, то верхняя полая вена легко спадается, и не выполняет своей основной функции.
Вторичные раковые образования в лимфатических узлах деформируют их и увеличивают в размерах, что способно нарушить проходимость вены. Через стенку вены прорастает опухоль средостения, что характерно для крайне агрессивных злокачественных лимфом и мелкоклеточного рака лёгкого. К опухолевому поражению может присоединиться венозный тромбоз, который возникает даже без опухолевого поражения средостения. К примеру, чрезвычайно способствуют повышенной свёртываемости крови злокачественные опухоли желудочно-кишечного тракта и рак яичников. Всё это — опухоль, тромб, метастазы в лимфатических узлах нарушают отток крови, вызывая венозный застой с отёком.

Диагностика синдрома верхней полой вены
С одной стороны диагностика синдрома верхней полой вены проста: внешний вид настолько специфичен, что диагноз ставится сразу, и на первый взгляд совершенно достаточно взглянуть на больного. Если больной имеет анамнез — историю онкогематологического или онкологического заболевания, когда есть данные гистологического исследования. Тогда ограничиваются констатацией всех зон опухолевого поражения и приступают к терапии. Но в половине случаев синдром верхней полой вены развивается в дебюте заболевания, то есть СПВП — первый и единственный явный признак злокачественной опухоли.
Необходимо выяснить, чем вызван синдром, и только тогда его лечить. О наличии злокачественной опухоли говорит морфологическое исследование кусочка опухоли, химиотерапия и лучевая терапия проводятся только при наличии морфологического подтверждения рака. Исключения из этого незыблемого правила есть и тяжёлые проявления синдрома верхней полой вены в их числе, тогда лечение проводится по жизненным показаниям до получения клеточного анализа. Тем не менее, в специализированных клиниках сегодня есть возможность срочно верифицировать — получить морфологическое подтверждение рака.
Всегда выполняется рентгенография органов грудной клетки с послойной томографией средостения, но лучше сделать компьютерную томографию. Исследования помогают сориентироваться с последующей диагностикой — где делать пункцию или брать биопсию. При подозрении на рак лёгкого выполняется исследование мокроты на клетки рака, биопсия при бронхоскопии, возможна пункционная биопсия средостенного лимфатического узла, эндоскопическое исследование средостения, при подозрении на злокачественную лимфому берут пункцию из подвздошной кости или грудины.
Получение гистологического материала начинают с простой диагностической методики, при неудаче обращаются к более сложной. Просто разобраться с диагнозом, если есть другие визуальные опухоли или увеличенные периферические лимфоузлы, откуда можно взять клетки для микроскопического исследования. Без понимания, какой злокачественный процесс вызвал синдром сдавления верхней полой вены невозможно подобрать оптимальное лечение, хотя в крайне тяжёлых случаях, когда под угрозой жизнь и промедление смерти подобно, вводят химиопрепараты широкого спектра, действующие на все возможные причины СВПВ.
Лечение синдрома верхней полой вены
Цель лечения — избавить больного от патологических симптомов, но на первом этапе главное — спасти ему жизнь. Понятно, что бессмысленно обращаться в общебольничную сеть и даже самую хорошую городскую реанимационную службу: пока доктора поймут, что это, и вызовут на консультацию онколога, а тот пригласит химиотерапевта и радиолога, уйдёт время, а состояние больного будет только ухудшаться. В Отечестве нет государственной «скорой онкологической помощи», только плановая госпитализация, что для больного первичным СВПВ крайне трагично, ведь ему нужна не просто онкология, а онкологическая реанимация.
Если СВПВ — первое проявление злокачественной опухоли, то перспективы терапии весьма неплохие, потому что высоко агрессивные мелкоклеточный рак лёгкого, злокачественная лимфома и герминогенные опухоли яичка потенциально излечимые заболевания, очень хорошо отвечающие на первую химиотерапию. В этом случае эффект первого введения цитостатика чудесным образом возвращает пациенту лицо, поскольку буквально за пару часов уходят тягостные проявления болезни.
При истории онкологического заболевания, когда уже пройдены и операция, и лучевая терапия на первичную опухоль, и несколько курсов химиотерапии по поводу метастазов, а СВПВ обусловлен дальнейшим прогрессированием рака, нет перспектив на излечение, но улучшить качество жизни и продлить её тоже возможно. Специализированная онкологическая реанимация обеспечит максимально возможное поступление воздуха в лёгкие, избавит от избыточной жидкости, снизит отёчность головного мозга, предупредит развитие судорог, минимизирует воздействие венозного застоя на сердце и в некоторых случаях уменьшит сдавление верхней полой вены подключением лучевой терапии на очаг в средостении.
При синдроме верхней полой вены у первичного онкологического больного успех обязателен, и даже при длительной истории рака успех возможен, надо только попасть туда, где не только знают, но и имеют возможность оказать квалифицированную экстренную и обязательно онкологическую помощь. Реанимационная служба Европейской клиники удовлетворяет этим высоким требованиям и готова спасать в любое время.
Тромбоз глубоких вен – причины, симптомы, диагностика, лечение
Тромбоз глубоких вен — заболевание, в основе которого лежит образование тромботических сгустков (тромбов) в просвете глубоких вен из-за нарушенного оттока крови, а также повышенная свертываемость крови, а также повреждение внутренней стенки вены. Наиболее часто тромбоз глубоких вен возникает в нижних конечностях.
В 3-15 % случаев данное заболевание вызывает летальный исход от тромбоэмболии лёгочной артерии (ТЭЛА).
Развитию тромбоза глубоких вен более подвержены мужчины. Однако данное заболевание не редкость и среди женщин, как осложнение приема гормональных контрацептивов.
— как осложнение хирургических операций (наркоза) и различных травм;
— длительная иммобилизация (гипсовая повязка, шина и т.д.) верхней и нижней конечности;
— длительное пребывание ног в согнутом положении (в автомобиле, самолёте, сидячая работа);
— избыточная масса тела и ожирение;
— в период беременности и в послеродовом периоде (из-за сдавления плодом нижней полой вены, а также магистральных вен таза);
— возраст пациента (малая подвижность, снижение тонуса вен, повышенная свертываемость крови);
— онкологические заболевания;
— заболевания печени (нарушение свертываемости крови);
— перенесенный венозный тромбоз в прошлом.
— выраженный отёк пораженной конечности;
— бледность кожных покровов конечности;
— боль распирающего характера (ощущение «боли в мышцах»);
— повышение температуры тела;
— общая слабость;
— увеличение в объеме подкожных вен.
Следует отметить, что при тромбозе вен голени не наступает значительных изменений венозного оттока, что утрудняет диагностику тромбоза глубоких вен.
Достаточно часто единственными симптомами тромбоза является незначительная боль в мышцах голени, которая усиливается при ходьбе.
— Доплерография магистральных вен нижних и верхних конечностей, вен таза, а также полых вен. Этот наиболее распространенный метод диагностики позволяет определить уровень тромбоза, наличие флотации тромба (угроза тромбоэмболии легочной артерии), а также давность процесса.
Главная цель в лечении тромбоза глубоких вен – предотвратить развитие тромбоэмболии легочной артерии.
Во многом тактика лечения зависит от конкретной локализации тромбов, наличия флотации, давности возникновения заболевания.
Программа лечения согласно рекомендациям Европейской ассоциации сосудистых хирургов:
— предотвратить дальнейшее распространение тромбоза глубоких вен;
— предотвратить развитие тромбоэмболии легочной артерии, которая может угрожать жизни пациента;
— предотвратить развитие отёка конечности;
— максимально восстановить проходимость магистральных вен, чтобы предотвратить развитие посттромбофлебитического синдрома;
— избежать развития рецидива тромбоза глубоких вен.

ЛЕЧЕНИЕ ВАРИКОЗА ЛАЗЕРОМ – ЭТО:
— возможность покинуть клинику сразу после процедуры;
— безопасность и малоинвазивность;
— отсутствие боли (манипуляция часто проводится под местной анестезией, иногда пациента погружают в медикаментозный сон);
— короткий период реабилитации;
— отсутствие осложнений;
— отсутствие рубцов и шрамов.
Стоимость консультации сосудистого хирурга, флеболога – 300 грн.
Запись по телефону: (067) 764-55-12



